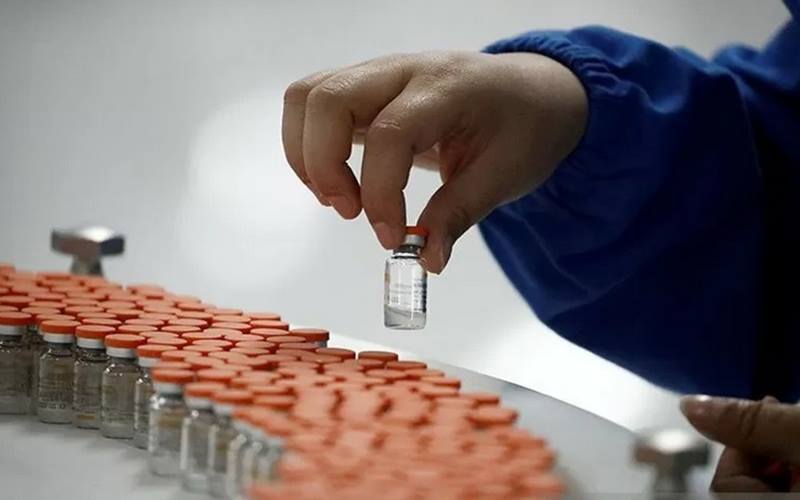
Bisnis.com, JAKARTA - Komite Penasihat Vaksin dan Produk Biologis (VRBPAC) di Badan Pengawas Obat dan Makanan Amerika Serikat atau FDA terlibat rapat virtual selama sembilan jam membahas izin penggunaan skala luas vaksin Covid-19 dengan hanya bukti efikasi dan keselamatan yang minimal.
Emergency use authorization (EUA), istilah yang belakangan menjadi populer tersebut, bisa hanya menggunakan data awalan dari uji klinis vaksin.
Karena akan memangkas proses berbulan-bulan dari pemberian persetujuan yang standar, kebijakan mengambil jalan pintas itu diserahkan FDA kepada VRBPAC untuk dikaji baik-buruknya.
Rapat dengar pendapat yang bisa diikuti lewat YouTube itu diikuti anggota komite terdiri dari akademisi, perwakilan konsumen, dan ilmuwan pemerintah.
Mereka berdebat alot tapi mengirim pesan yang cukup jelas kepada FDA: tahan diri.
Beberapa anggota VRBPAC mencemaskan pemberian izin darurat bisa berkontribusi kepada semakin berkembangnya keraguan publik terhadap vaksin Covid-19.
Ini karena ikut berkembang adanya persepsi bahwa FDA telah mengkompromikan standarnya yang sudah terkenal tinggi.
Sheldon Toubman, seorang pengacara yang mewakili kepentingan konsumen di komite itu, menyerukan kepada FDA untuk tidak menerbitkan EUA bagi vaksin Covid-19.
Alasannya, FDA harus tetap pada prosedur persetujuan yang sudah ada demi menghindari bertambahnya masalah kurangnya kepercayaan publik kepada vaksin.
"Hanya ada satu kesempatan untuk melakukannya dengan benar," katanya dalam rapat Kamis (22/10/2020).
Dia menambahkan, "Dan jika kita melakukannya dengan salah, maka selesailah semua untuk bertahun-tahun ke depan yang membuat kita sulit lagi ke luar."
Komite FDA itu juga mendiskusikan kemungkinan izin terlalu dini dari sebuah vaksin dapat mengganggu banyak uji coba vaksin Covid-19 yang masih berjalan saat ini, memoraporandakan upaya mendapatkan data efikasi dan keselamatan yang paling tegas dan meyakinkan.
Dan beberapa anggota komite khawatir panduan paling terkini dari FDA utuk perusahaan vaksin yang mencari izin penggunaan darurat belum memiliki kriteria keselamatan yang cukup ketat.
Sebanyak empat kandidat vaksin terpilih dalam Operation Warp Speed--program percepataan pengadaan Vaksin Covid-19 di Amerika Serikat--sedang dalam uji klinis terhadap sedikitnya 30 ribu relawan.
Uji klinis menggunakan metode buta di mana setiap relawan tidak tahu apakah suntikan yang dberikan kepada mereka menerima vaksin atau plasebo.
Mereka didesain untuk berhenti ketika memiliki sekitar 150 kasus sakit, tapi badan pemantau independen akan memberitahu para penyelidik apakah sebuah vaksin kelihatannya bekerja baik pada 50 kasus dan lagi pada 100 kasus.
Panduan yang dikeluarkan FDA pada Juni lalu menyatakan badan itu akan mempertimbangkan menerbitkan EUA untuk sebuah vaksin jika hasilnya menunjukkan efikasi sedikitnya 50 persen di setiap analisis itu.
Presiden Donald Trump telah berulang kali mendorong adanya izin penggunaan darurat untuk sebuah vaksin Covid-19 sebelum pelaksanaan pilpres 3 November, tapi FDA telah menepisnya.
FDA mengeluarkan panduan kedua yang menambahkan sebuah syarati keselamatan: harus sudah berselang dua bulan sejak sedikitnya separuh jumlah orang dalam uji coba menerima seluruh dosis yang direncanakan, untuk melihat apakah ada efek samping yang muncul.
Beberapa anggota komite dan pakar menilai dua bulan belum cukup panjang dan meminta FDA menambahnya jadi sedikitnya enam bulan.